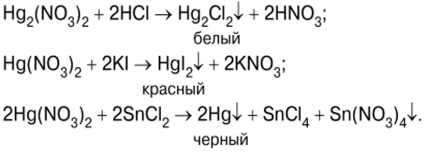
பாதரச கலவைகளின் எதிர்வினைகள்
உலோக பாதரசம் மற்றும் அதன் கலவைகள் உயிரினங்களுக்கு மிகவும் நச்சுத்தன்மை வாய்ந்தவை. தண்ணீரில் அதிகம் கரையக்கூடிய கலவைகளுக்கு இது குறிப்பாக உண்மை. இந்த தனித்துவமான தனிமத்தின் சேர்க்கைகளை பரிசோதிக்கும் போது மிகவும் கவனமாக இருக்க வேண்டும் (அறை வெப்பநிலையில் திரவமாக இருக்கும் ஒரே உலோகம் பாதரசம்). வேதியியலாளரின் அடிப்படை விதிகளுக்கு இணங்கவா? பாதரச கலவைகளுடன் பல சோதனைகளை பாதுகாப்பாக நடத்த உங்களை அனுமதிக்கும்.
முதல் பரிசோதனையில், நாம் அலுமினிய அமல்கம் (திரவ பாதரசத்தில் இந்த உலோகத்தின் தீர்வு) பெறுகிறோம். பாதரசம் (II) கரைசல் Hg நைட்ரேட் (V) Hg (NO3)2 மற்றும் அலுமினிய கம்பியின் ஒரு துண்டு (புகைப்படம் 1). ஒரு கரையக்கூடிய பாதரச உப்பு (புகைப்படம் 2) ஒரு தீர்வுடன் ஒரு சோதனைக் குழாயில் ஒரு அலுமினிய கம்பி (கவனமாக வைப்புகளை சுத்தம் செய்தல்) வைக்கப்படுகிறது. சிறிது நேரம் கழித்து, கம்பியின் மேற்பரப்பில் இருந்து வாயு குமிழ்கள் வெளிவருவதை நாம் அவதானிக்கலாம் (புகைப்படங்கள் 3 மற்றும் 4). கரைசலில் இருந்து தடியை அகற்றிய பிறகு, களிமண் ஒரு பஞ்சுபோன்ற பூச்சுடன் மூடப்பட்டிருக்கும் என்று மாறிவிடும், கூடுதலாக, உலோக பாதரசத்தின் பந்துகளையும் நாங்கள் காண்கிறோம் (புகைப்படங்கள் 5 மற்றும் 6).
வேதியியல் - பாதரசத்தை இணைக்கும் அனுபவம்
சாதாரண நிலைமைகளின் கீழ், அலுமினியத்தின் மேற்பரப்பு அலுமினிய ஆக்சைடு இறுக்கமாக பொருத்தப்பட்ட அடுக்குடன் பூசப்படுகிறது.2O3ஆக்கிரமிப்பு சுற்றுச்சூழல் தாக்கங்களிலிருந்து உலோகத்தை திறம்பட தனிமைப்படுத்துகிறது. பாதரச உப்பின் கரைசலில் கம்பியை சுத்தம் செய்து மூழ்கடித்த பிறகு, Hg அயனிகள் இடம்பெயர்கின்றன.2+ அதிக செயலில் உள்ள அலுமினியம்
தடியின் மேற்பரப்பில் படிந்த பாதரசம் அலுமினியத்துடன் ஒரு கலவையை உருவாக்குகிறது, இது ஆக்சைடு அதை ஒட்டிக்கொள்வதை கடினமாக்குகிறது. அலுமினியம் மிகவும் சுறுசுறுப்பான உலோகமாகும் (இது ஹைட்ரஜனை வெளியிட தண்ணீருடன் வினைபுரிகிறது - வாயு குமிழ்கள் கவனிக்கப்படுகின்றன), மேலும் அடர்த்தியான ஆக்சைடு பூச்சு காரணமாக அதன் கட்டமைப்புப் பொருளாக இது சாத்தியமாகும்.
இரண்டாவது பரிசோதனையில், அம்மோனியம் NH அயனிகளைக் கண்டறிவோம்.4+ நெஸ்லரின் மறுஉருவாக்கத்தைப் பயன்படுத்தி (ஜெர்மன் வேதியியலாளர் ஜூலியஸ் நெஸ்லர் 1856 இல் பகுப்பாய்வில் இதைப் பயன்படுத்தினார்).
ஹாப்ஸ் மற்றும் பாதரச கலவைகளின் எதிர்வினை பற்றிய பரிசோதனை
சோதனையானது பாதரசம்(II) அயோடைடு HgI இன் மழைப்பொழிவுடன் தொடங்குகிறது.2, பொட்டாசியம் அயோடைடு KI மற்றும் பாதரசம் (II) நைட்ரேட் (V) Hg (NO) ஆகியவற்றின் கரைசல்களைக் கலந்த பிறகு3)2 (புகைப்படம் 7):
HgI இன் ஆரஞ்சு-சிவப்பு படிவு2 (புகைப்படம் 8) பின்னர் அதிகப்படியான பொட்டாசியம் அயோடைடு கரைசலைக் கொண்டு சிகிச்சையளித்து, கே சூத்திரத்தின் கரையக்கூடிய சிக்கலான கலவையைப் பெறலாம்.2HgI4 ? பொட்டாசியம் டெட்ராயோடர்குரேட் (II) (புகைப்படம் 9), இது நெஸ்லரின் வினைப்பொருள்:
இதன் விளைவாக வரும் கலவை மூலம், அம்மோனியம் அயனிகளை நாம் கண்டறிய முடியும். சோடியம் ஹைட்ராக்சைடு NaOH மற்றும் அம்மோனியம் குளோரைடு NH ஆகியவற்றின் தீர்வுகள் இன்னும் தேவைப்படும்.4Cl (புகைப்படம் 10). நெஸ்லர் மறுஉருவாக்கத்தில் ஒரு சிறிய அளவு அம்மோனியம் உப்பு கரைசலைச் சேர்த்து, நடுத்தரத்தை ஒரு வலுவான அடித்தளத்துடன் காரமாக்கிய பிறகு, சோதனைக் குழாயின் உள்ளடக்கங்களின் மஞ்சள்-ஆரஞ்சு நிறத்தை உருவாக்குவதை நாங்கள் கவனிக்கிறோம். தற்போதைய எதிர்வினை பின்வருமாறு எழுதலாம்:
இதன் விளைவாக பாதரச கலவை ஒரு சிக்கலான அமைப்பைக் கொண்டுள்ளது:
அதிக உணர்திறன் கொண்ட நெஸ்லர் சோதனையானது தண்ணீரில் அம்மோனியம் உப்புகள் அல்லது அம்மோனியாவின் தடயங்களைக் கூட கண்டறியப் பயன்படுகிறது (எ.கா. குழாய் நீர்).

